DIE AKUTE MENINGITIS
Univ.-Prof. Dr. Erich Schmutzhard,
Univ.-Klinik für Neurologie, Universität Innsbruck
erich.schmutzhard@uibk.ac.at
![]()
Definition
Eine akute purulente Meningitis ist eine akute (bis subakute) Infektion der Leptomeningen, die durch, die Bluthirnschranke überwindende, Bakterien oder, in seltenen Fällen, Protozoen (freilebende Amoeben) - siehe 1.1.2. - verursacht wird und mit charakteristischen chemischen und zellulären Veränderungen des Liquor cerebrospinalis vergesellschaftet ist.
Theoretisch kann jedes Bakterium eine akute Meningitis
verursachen, die wichtigsten bakteriellen Erreger einer community
akquirierten bakteriellen Meningitis sind:
* Haemophilus influenzae Typ
B (HiB)
* Neisseria meningitidis (Meningokokken) und
* Streptococcus
pneumoniae (Pneumokokken).
Nicht bakterielle Erreger einer purulenten Meningitis sind freilebende Amoeben der Spezies Naegleria fowleri.
Epidemiologie
Die Inzidenz der akuten purulenten Meningitis beträgt 3-10/100.000 Menschen pro Jahr. Im ersten Lebensmonat ist die altersspezifische Inzidenz am höchsten, ca. 2/3 aller sporadischen purulenten Meningitisfälle werden bei Kindern unter 5 Jahre beobachtet, ca. 3/4 aller purulenten Meningitisfälle bei Kindern und Jugendlichen unter 15 Jahren. Es besteht ein leichtes Überwiegen weiblicher Patienten (m:w = 1:1,7). Neben den Alters- und Geschlechtsunterschieden sind vor allem geographische Unterschiedlichkeiten, sowohl in der Inzidenz als auch im Erregerspektrum, besonders hervorzuheben.
Während Meningokokken die einzigen Erreger sind, die größere bzw. bedrohliche Epidemien einer bakteriellen Meningitis verursachen, können sporadisch auftretende purulente Meningitiden theoretisch von jedem bakteriellen Erreger ausgelöst werden.
Die relative Häufigkeit, mit der die einzelnen Bakterienspezies eine purulente Meningitis verursachen, ist eindeutig altersabhängig. E. coli, Gruppe B Streptokokken, Listeria Spezies, sowie Pseudomonas Spezies spielen bei Neugeborenen (< 1 Monat) eine überwältigende Rolle. Bei Kindern wurde bis zur Einführung der akuten Immunisierung gegen HiB dieser Meningitiserreger am häufigsten gesehen, bei ausreichendem HiB Durchimpfungsgrad sind derzeit Meningokokken, aber auch Pneumokokken die häufigsten Meningitiserreger bei den unter 15jährigen. Im höheren Lebensalter sind Pneumokokken (bis zu 50% aller Meningitisfälle), seltener Meningokokken, sowie Listerien die häufigsten Erreger der community akquirierten Meningitis (in dieser Reihenfolge).
Tabelle 1 listet die altersbezogenen prädisponierenden Faktoren:
| Altersabhängige prädisponierende Faktoren für eine akute bakterielle Meningitis | Alter < 5 a | Erwachsene |
| Sichelzellenerkrankung | + | |
| Immunglobulindefizienz | + | + |
| Splenektomie | + | + |
| Z.n. Schädelhirntrauma, Liquorleck | + | + |
| paranasale Infektion (Sinusitis, Otitis) | + | + |
| Pneumonie | + | |
| Diabetes mellitus | + | |
| chronische Alkoholkrankheit | + |
Pathogenese
Eine bakterielle community akquirierte Meningitis durch die drei wichtigsten Erreger (HiB, Meningo-kokken und Pneumokokken, i.e. enkapsulierte Mikroorganismen) läuft entsprechend einer typischen Abfolge von Ereignissen ab: die initiale Kolonisierung der Schleimhaut des oberen Respirationstraktes wird von einer hämatogenen Streuung gefolgt, die Bluthirnschranke wird penetriert und die Erreger vermehren sich letztlich im Liquor-/Subarachnoidalraum. Die Polysaccharidkapsel ist typisch für die wichtigsten 3 Meningitiserreger (HiB, Meningokokken, Pneumokokken), aber auch für E. coli oder Gruppe B Streptokokken (siehe Neugeborenenmeningitis). Diese Kapselbildung ist ein wesentlicher Schutzmechanismus vor der Phagozytose durch neutrophile Granulozyten und inhibiert auf verschiedene Weisen die antikörperunabhängige komplementmediierte bakterizide Aktivität. Im Affenexperiment konnte gezeigt werden, dass die initiale Eintrittspforte von HiB in das zentrale Nerven-system der Plexus chorioideus ist, der die frühesten histopathologischen Entzündungszeichen zeigt. Nach dem Verlassen der entzündlich veränderten Plexus chorioideus Kapillaren invadieren die Erreger die Seitenventrikel und letztlich den Subarachnoidalraum.
Mikrobiologie
Obwohl geographische/regionale Unterschiede bestehen, sind weltweit gesehen ca. 75-80% aller community akquirierten bakteriellen Meningitiden den großen drei zuzuordnen: Haemophilus influenzae Typ B (HiB), Neisseria meningitidis (Meningokokken) und Streptococcus pneumoniae (Pneumokokken), wenngleich die unterschiedliche Gewichtung dieser Erreger nicht nur geographisch, sondern auch im Verlauf der Zeit durch gesundheitspolitische Maßnahmen (z.B. HiB-Impfung) beeinflusst wurde.
Tabelle 2 listet die altersspezifische Häufigkeit der wichtigsten Erreger auf:
| Altersspezifische Häufigkeit der wichtigsten Erreger einer akuten bakteriellen Meningitis | |||
|
Erreger |
< 1Monat, % |
1 Monat bis 15 Jahre, % |
> 15 Jahre, % |
| H. influenzae | 0-3 | 50 | 1-3 |
| Meningokokken | 0-1 | 30 | 25 |
| Pneumokokken | 0-5 | 15 | 40 |
| Gramnegative | 50 | 1-2 | 1-10 |
| Bakterien | |||
| Streptokokken | 30 | 2-4 | 5 |
| Staphylokokken | 5 | 1-2 | 1-15 |
| Listerien | 1-10 | 1-2 | 5 |
Einteilung der Meningokokken in Serogruppen und Subtypen
Die Klassifizierung in Serogruppen beruht auf strukturelle Unterschiede in den Kapselpolysacchariden sowie auch unterschiedliche Agglutinationsreaktionen mit spezifischen Antisera. Die Serogruppen-klassenfizierung hat epidemiologische und gesundheitspolitische Implikationen. Derzeit sind 13 Sero-gruppen bekannt: A, B, C, D, H, I, K, L, X, Y, Z, 29E und W135. Serogruppen A, B, C, Y und W135 stellen den überwiegenden Anteil an Meningokokkenerkrankungen. In Mitteleuropa spielen vor allem Serogruppe B Meningokokken (in jüngsten Jahren auch Serogruppe C) eine wesentliche Rolle, während im sogenannten Meningitisgürtel Afrikas, aber auch in Nordindien und Nepal die letzten Epidemien durch Serogruppe A Meningokokken bedingt waren.
Symptomatik
Neurologische Symptomatik ( siehe Tabelle 3)
Mehr als die Hälfte der Patienten mit einer community
akquirierten bakteriellen Meningitis berichten über Symptome des oberen
Respirationstraktes im Sinne eines grippalen Infektes, einer Pharyngitis
oder auch Otitis media, die der eigentlichen Erkrankung vorausgehen. Der
Übergang in die meningitische Symptomatik geht bei bis zu 50% der
Patienten in einem Zeitraum von 1-7 Tagen vor sich, so dass die
Frühdiagnose bei diesen Patienten oft schwierig zu stellen ist. In den
übrigen 50
(-75%) der Patienten ist der Krankheitsbeginn akut bis
perakut mit einer Dauer von wenigen Stunden bis 1 Tag. Nach einer kurzen
Phase von uncharakteristischen Symptomen wie Nausea, allgemeines
Krankheitsgefühl, Muskelschmerzen entwickelt sich ein charakteristischer
Symptomenkomplex, der als meningeales Syndrom bezeichnet wird.
Meningeales Syndrom (charakteristischer Symptomenkomplex)
* Kopfschmerzen
* Photophobie
* Nackensteifigkeit
bis zum Opisthotonus
* positives Laséguezeichen
* positives
Kernigzeichen und positives Brudzinskizeichen
* vegetative
Störungen
* Hyperpathie der Haut
* im Verlauf - psychomotorische
Beeinträchtigung
Die klassische Trias der bakteriellen Meningitis mit Nackensteifigkeit, Fieber und Veränderung der Bewußtseinslage findet man bei maximal 2/3 der Patienten mit community akquirierter bakterieller Meningitis. Allerdings ist in nahezu allen Fällen zumindest eines der drei Symptome deutlich ausgeprägt.
Zum Zeitpunkt der ersten Untersuchung weisen 80% der erwachsenen Patienten mit bakterieller Meningitis eine Beeinträchtigung des Bewußtseins oder der Bewußtheit auf. Ca. die Hälfte der Patienten sind zu diesem Zeitpunkt verwirrt, desorientiert oder somnolent, 1/5 der Patienten zeigt einen Sopor, nur auf stärkere äußere Reize bzw. Schmerzreize antwortend/reagierend, mindestens 5% der Patienten sind zum Zeitpunkt der ersten Untersuchung bereits komatös. Das Ausmaß der Bewußtseinsstörung zum Zeitpunkt des Therapiebeginns beeinflusst eindeutig die Prognose. Neben der Beeinträchtigung der Bewußtseinslage sind beim Erwachsenen, insbesondere bei Pneumokokken-meningitis und bei Kindern mit HiB Meningitis, bei nahezu einem Drittel der Patienten tonisch klonisch generalisierte Anfälle zu beobachten. Bei 10-20% der Patienten, häufiger bei Pneumokokken als HiB oder Meningokokkenmeningitis, finden sich fokale neurologische Ausfälle. Nur selten treten neurologische Herdsymptome in der Frühphase der bakteriellen Meningitis (insbesondere Pneumo-kokkenmeningitis) auf, eventuell als sogenannte Todd'sche Parese nach einem fokal eingeleiteten, sekundär generalisierten tonisch klonischen Anfall. Erst im Verlaufe einer bakteriellen (bes. Pneumo-kokken) Meningitis (Tag 4-7) finden sich vaskulär-ischämisch bedingte Herdsymptome (bei Arteritis) bzw. Herdsymptome (und eventuell auch fokale und/oder generalisierte tonisch klonische Anfälle) als Folge einer septischen Sinusvenenthrombose. Ca. ein Drittel aller intrakraniellen Komplikationen sind zerebrovaskulärer Natur, sie inkludieren Vasospasmus, vaskulitische Verschlüsse, aneurysmatische Ausweitungen, Extravasation des Kontrastmittels sowie Thrombose der kortikalen Venen oder der zerebralen Sinus. Ein diffuses Hirnödem, ein Hydrocephalus occlusus oder aresorptivus führt zur raschen Entwicklung der klinischen Symptome eines erhöhten Hirndrucks mit Störung der Pupillomotorik, der Optomotorik, dem Auftreten von Koma, vegetativen Symptomen (Bradykardie, Atem-regulationsstörung) und letztlich dem Auftreten von Dekortikations- und Dezerebrationsmustern. Aufgrund der raschen Dynamik mit der sich die Hirndruckerhöhung entwickelt, ist fundoskopisch praktisch nie eine Stauungspapille zu sehen. Das Vorhandensein einer solchen weist immer auf andere eigenständige oder auch mit der aktuellen Infektionskrankheit in Zusammenhang stehende Erkrankung wie subdurales Empyem oder Hirnabszess hin.
Andere Organmanifestationen (siehe Tabelle 3)
25-50% der erwachsenen Patienten mit Pneumokokkenmeningitis zeigen zum Zeitpunkt der Aufnahme eine Pneumonie. Eine Otitis media oder paranasale Sinusitis wird bei bis zu zwei Drittel der Pneumo-kokkenmeningitis-Patienten gesehen. Andere parameningeale infektiöse Foci oder ein Liquorleck nach Schädelhirntrauma sind ebenfalls wesentliche prädisponierende Faktoren.
Petechien oder eine Purpura fulminans, die hauptsächlich im Bereich der Extremitäten, aber auch - ins-besondere im Verlaufe - am Stamm lokalisiert sind, letztlich im Bereich der Schleimhäute ebenfalls zur Beobachtung kommen, weisen in Zusammenhang mit Fieber und Meningismus und dem typischen Alter (2-6 Jahre bzw. 14-20 Jahre) unter allen Umständen auf eine Meningokokkenerkrankung hin. Ca. 50% aller Patienten mit einer Meningokokkenmeningitis zeigen diese Hautveränderungen. Bei schweren Verläufen entwickeln sich Nekrosen der Haut, eventuell Gangrän von Zehen, Fingern und in seltenen Fällen der Extremitäten. 10-20% der Patienten mit einer Meningokokkeninfektion (Meningitis plus Bakteriämie) entwickeln ein Waterhouse-Friderichsen-Syndrom, das durch den plötzlichen Beginn einer fieberhaften Erkrankung, großen konfluierenden Petechien und Ekchymosen der Haut- und Schleimhäute, inklusive Gangränentwicklung der Extremitäten oder Finger/Zehen gekennzeichnet ist, außerdem besteht ein septischer Schock mit massivster Hypotonie, Tachykardie, eine schwerste disseminierte intravasale Gerinnungsstörung und eine Nebennierennekrose.
Tabelle 3 - Typische neurologische und allgemeine/systemische Symptomatik bei bakterieller Meningitis
|
Alter |
Neurologische Symptomatik |
systemische Symptomatik |
| < 5 Jahre |
Meningismus |
Fieber Zeichen einer Infektion des oberen Respiraltraktes Petechien oder Purpura Veränderung von: Qualität des Schreiens Hautfarbe Hydrationszustand Antwort auf sozialen Stimulus |
| 15-50 Jahre | Meningismus Veränderung der Bewusstseinslage Desorientiertheit, Verwirrtheit Erbrechen, Nausea Photophobie Hirnnervenläsionen |
Fieber Symptome des oberen Respirationstraktes Petechien/Purpura Sepsissyndrom |
| > 50 Jahre | Meningismus Desorientiertheit, Verwirrtheit Bewusstseinstrübung - Koma Kopfschmerzen zerebrale Krampfanfälle bis zum Status epilepticus neurologische Herdsymptome Hirnnervenläsionen Hirnstammsymptomatik |
Fieber Symptome des oberen Respirationstraktes Sepsissyndrom |
Diagnostik
Neurologische Diagnostik
Eine bakterielle Meningitis muss bei jedem Patienten mit der typischen Trias des meningealen Syndroms - Nackensteifigkeit, Fieber, Veränderung der Bewusstseinslage - vermutet werden. Bei älteren Menschen, bei bestimmten Erregern (gramnegative), sowie bei komatösen Patienten können allerdings der typische Meningismus und die meningealen Irritationszeichen fehlen. Nur zwei Drittel der Patienten mit community akquirierter bakterieller Meningitis zeigen diese klassische Trias, allerdings ist praktisch in jedem Fall zumindest eines dieser drei Symptome deutlich ausgeprägt.
Lumbalpunktion
Zur Sicherung der Diagnose einer bakteriellen Meningitis ist die Lumbalpunktion essentiell. Allerdings muss bei Vorhandensein einer Bewusstseinsstörung (Verdacht auf erhöhte intrakraniellen Druck) und insbesondere bei eindeutig fassbaren neurologischen Herdsymptomen (Verdacht auf Hirnabszess, subdurales Empyem) einer Lumbalpunktion eine bildgebende Untersuchung, z.B. eine cerebrale Computertomographie, vorausgehen. Die in der Diagnostik der akuten bakteriellen Meningitis wesentlichen Liquorparamter sind in Tabelle 4 aufgelistet.
Tabelle 4
| Akute Phase | Proliferationsphase (subakut) | Reparationsphase | |
| Farbe | eitrig trüb | trüb bis klar | klar |
| Zellzahl | zu Beginn evtl. <
300/µl rasch > 1000/µl |
> 100/µl | 30-90/µl |
| Zellbild | überwiegend segmentkernige, neutrophile Granulozyten, auch monozytäre und histioretikuläre Zellen, selten lymphozytäre Zellen | Abfall der segmentkernigen Granulozyten, Anstieg der monozytären und lymphozytären Zellen, einzelne Plasmazellen | gemischtzellig, lymphozytäre Zellen |
| Eiweiß | > 100 mg/dl | ca. 100 mg/dl | normal |
| Zucker | < 40 mg/dl | Normalisierung | normal |
| Liquor/Serum | < 0,4 | < 0,4 | normal |
| Glukose-Ratio | |||
| Laktat | > 3,8 mmol/l | Normalisierung | normal |
Mikrobiologische Diagnostik
Bei der akuten bakteriellen Meningitis muss bei der Lumbalpunktion immer auch die Asservierung einer maximal sterilen Probe zur Liquorkultur gefordert werden. Während bei unbehandelten Patienten mit bakterieller Meningitis das Ergebnis der Liquorkultur in 70-90% ein positives Ergebnis bringt, sinkt dieser Prozentsatz nach antibiotischer Vorbehandlung auf 30-50%. Neben der Liquorkultur sind bei Patienten mit community akquirierter Meningitis auch Blutkulturen und Rachenspülflüssigkeitskulturen vor dem Beginn der antibiotischen Therapie zu gewinnen. Die Untersuchung des Liquors mittels Gramfärbung erlaubt eine rasche und akkurate Identifizierung des Erregers. Wenn der Liquor trüb ist, wird er zur Gramfärbung nativ verwendet, bei klarem Liquor sollte er vor der Gramfärbung zentrifugiert werden.
Während des Krankheitsverlaufes sind folgende Symptome unbedingte Indikationen zur Durchführung einer zerebralen CT (oder MRT):
* persistierendes Fieber
* neu sich entwickelndes
Fieber
* prolongiertes neurologisches Defizit oder
Bewußtseinstrübung
* neu auftretende rezidivierende zerebrale
Anfälle
* Zeichen des erhöhten Hirndrucks
* Neuentwicklung fokaler
neurologischer Defizite
Typische CT-Befunde:
* Anspeicherung der Leptomeningen
und des Ventrikelependyms
* Hirnödem mit Verstreichung der
Gyri-Sulci-Zeichnung und Aufhebung des kortikomedullären Kontrastes
*
in Einzelfällen - ein Hydro-/Pyocephalus
Komplikationen
Neurologische und nicht neurologische Komplikationen tragen zur nach wie vor beträchtlichen Morbidität und Mortalität der community akquirierten bakteriellen Meningitis bei. Nur knapp mehr als die Hälfte der Patienten wird nach einer bakteriellen Meningitis wieder vollständig hergestellt sein. Akute Komplikationen (Frühkomplikationen), die in den ersten wenigen Tagen der akuten bakteriellen Meningitis auftreten, intermediäre Komplikationen, die nach 3-8 Tagen typischerweise den Verlauf prägen und Langzeitkomplikationen, die auch nach mikrobiologischer vollständiger Heilung perisistieren, erschweren den Krankheitsverlauf.
Neurologische und nicht neurologische Komplikationen stellen gleichermaßen oft unüberwindliche Anforderungen an das Behandlungsteam. In einem unselektionierten Patientengut von 86 konsekutiven adulten Meningitisfällen traten bei 15,1% zerebrovaskuläre Komplikationen auf, bei 14% ein Hirnödem, bei je 11,6% ein Hydrocephalus und septisches Schockgeschehen, bei 8,1% eine disseminierte intravasale Koagulopathie, 8,1% entwickelten eine transtentorielle Herniation und bei 3,5% verkompli-zierte ein ARDS den Verlauf. Insbesondere früh im Krankheitsverlauf sind bestimmte bakterielle Erreger typisch für einzelne Komplikationen (Tabelle 5).
Tabelle 5 - Komplikationen und deren typische Erreger der akuten bakteriellen Meningitis
|
Komplikation |
typische Erreger |
| Hörverlust/Taubheit | HiB, Meningokokken, Streptococcus suis |
| Anfälle | Pneumokokken, HiB, Gruppe B Streptokokken |
| Neurologische Herdsymptomatik (vaskulär/ischämisch) | Pneumokokken |
| Hirnvenen/Sinusvenenthrombose | HiB (Haemophilus influenzae Typ B) |
| Hydrocephalus | HiB, Gruppe B Streptokokken, Pneumokokken |
| Hirnnervenläsionen | Meningokokken, Listerien |
| Panophtalmitis | Meningokokken, Pneumokokken, HiB |
| Subduraler Erguss | HiB, Pneumokokken |
| Septische Arthritis | Meningokokken, Staphylococcus aureus |
| Herpes labialis | Pneumokokken, Meningokokken |
| Purpura, Petechien | Meningokokken, Pneumokokken, Listerien |
| Schocksyndrom | Meningokokken, andere gramnegative Bakterien |
Differentialdiagnose
Tabelle 6 listet die wesentlichen Differentialdiagnosen der akuten bakteriellen Meningitis auf:
Tabelle 6
|
Diagnose |
differentialdiagnostisches
Stichwort |
differentialdiagnostische
Untersuchung |
| Virale Meningitis | saisonale Verteilung, Leukozyten, CRP, Liquor | Liquor, Blutbild, CRP |
| akute syphilitische Meningitis | Schanker, makulopapulöses Exanthem, generalisierte Lymphadenopathie | Liquor, TPHA, VDRL |
| Neuroborreliose | Zeckenstich, Erythema migrans, saisonale Verteilung | Liquor, Serologie |
| Leptospirenmeningitis | Exposition, biphasischer Verlauf, Konjunktivitis | Liquor, Serologie |
| Rickettsien | Exposition, Arthropodenstich, Hautmanifestation | Hautbiopsie |
| Tuberkulöse Meningitis | Exposition, Krankheitsverlauf (subakut bis chronisch) | Liquor, deutlich erhöhtes Liquor-eiweiß, Bildgebung: basale Meningitis, Hydorcephalus |
| Pilzmeningitiden | subakut bis chronisch, Exposition; Immunsuppression | Liquor, Tuschepräparat, Antigen-Detektion |
| Akute purulente Meningitis durch frei-lebende Amoeben (Naegleria fowleri) | Schwimmbadexposition, Jahreszeit (Sommer), warmes Klima | ausschließlich Granulozyten, negative Gramfärbung im Liquor; Trophozoiten im Nativ-Liquor |
| Septische Herdenzephalitis bei bakterieller Endokarditis | embolische Hirninfarkte, mykotische Aneurysmen | Bildgebung, Blutkultur, Echokardiographie, Gramfärbung aus Hautabstrichen |
| Chemische Meningitis | Kraniopharyngeom, Epidermoidtumor (insbes. hintere Schädelgrube) | Bildgebung |
| Hypersensitivitätsreaktion (eine Meningitis ist in seltenen Fällen das führende Symptom) | Medikamentenexposition | Anamnese, Eosinophilie |
| Systemischer Lupus | Grundkrankheit, Hautläsionen | antinukleäre Antikörper |
| erythematodes Behcet-Syndrom | urogenitale Ulzera, Uveitis, Arthritis | HLA B 27 |
| Mollaret-Meningitis | rezidivierende mononukleäre Pleozytose | epitheliale/endotheliale Zellen im Liquor |
| Hirnabszess | initiale Herdsymptomatik | Bildgebung, Cave: Lumbalpunktion |
| Epi-, subdurales Empyem | frühzeitig ausgeprägte Herdsympto-matik, einseitiger Kopfschmerz | Bildgebung, Cave: Lumbalpunktion |
| Septische Sinusvenenthrombose | parameningeale Infektion, hämorrhagische venöse Infarzierung | Bildgebung, Kernspintomographie, evtl. zerebrale Panangiographie |
| Zerebrale Malaria | Tropenaufenthalt, Fiebertyp, normale Leukozytenzahl | Blutausstrich |
| malignes Neuroleptikasyndrom | Neuroleptikatherapie, Rigor aller Extremitäten, Rhabdomyolyse | CPK, Myoglobinurie |
| Subarachnoidalblutung | plötzliche Kopfschmerzen, kein Fieber | zerebrale Computertomographie, blutiger (xantochromer) Liquor, zerebrale Pan-angiographie |
Therapie bzw. Management
Die Tabellen 7-11 listen die empirischen bzw. fokussierte antibiotische Therapie und ihre Dosis. Abb. 1 stellt den empfohlenen Management-Algorithmus dar.
Abbildung 1 - Empfohlener Management-Algorithmus
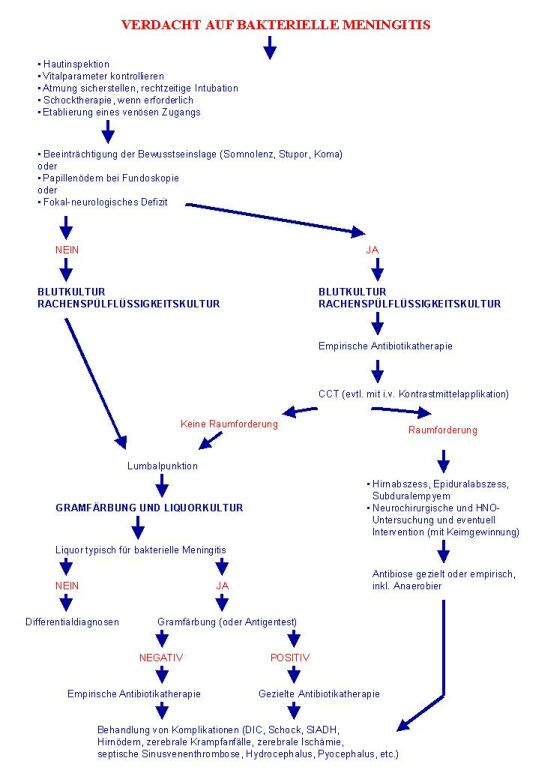
Tabelle 7 - Antibiotische Therapie der bakteriellen Meningitis, Alter als Hinweis für Erreger
|
Alter |
antibiotische Therapie |
Erreger |
| 0-4 Wochen | Ampicillin + Cefotaxim oder Ampicillin + Aminoglycosid | Gruppe B Streptokokken, E. coli, Listerien |
| 4 Wochen - 3 Monate | Ampicillin + Cefotaxim/Ceftriaxon | Gruppe B Streptokokken, E. coli, Listerien, H. influenzae |
| 3 Monate - 18 Jahre | Penicillin G oder Cefotaxim/Ceftriaxon | Neisseria meningitidis, Streptococcus pneumoniae H. influenzae |
| > 18 Jahre | Penicillin G oder Cefotaxim/Ceftriaxon | Neisseria meningitidis, Streptococcus pneumoniae |
| > 50 Jahre | Ampicillin + Cefotaxim/Ceftriaxon | Streptococcus pneumoniae, Listerien, Neisseria meningitidis, gramnegative Stäbchen |
Tabelle 8 - Zugrundeliegende Erkrankung oder begleitende Akutsymptomatik als Hinweis auf bestimmte Erreger (antibiot. Therapie, siehe Tabelle 11)
| AIDS | Listerien, Nokardien, Mycobacaterium tuberculosis |
| Alkoholismus | Streptococcus pneumoniae |
| Baden im Süsswasser | Amoeben |
| Defekt der zellulären Immunität | Listeria monocytogenes, gramnegative Stäbchen |
| Dermalsinus | Gramnegative Stäbchen, Staphylokokken |
| Diabetes mellitus | Streptococcus pneumoniae, Enterococcus, gramnegative Stäbchen, Staphylokokken |
| Endokarditis | Streptococcus pneumoniae, Enterococcus, Staphylococcus aureus, Bacteroides spp. |
| Familiäre Belastung | Neisseria meningitidis, Haemophilus influenzae |
| Gehirnabszess | Anaerobier, Citrobacter (Kinder), Staphylococcus aureus, Enterobacteriaceae |
| Hautblutungen | Neisseria meningitidis |
| Hypogammaglobulinämie | Neisseria meningitidis, Streptococcus pneumoniae, Haemophilus influenzae |
| Intensivpatient | Gramnegative Stäbchen, Staphylococcus aureus |
| Intrakranialer Shunt | Staphylococcus epidermidis, Staphylococcus aureus, Gramnegative Stäbchen |
| Intravenöser Drogenmissbrauch | Staphylococcus aureus, andere Staphylokokken, Gramnegative Stäbchen, Enterococcus, Pseudomonas aeruginosa |
| Leukämie | Gramnegative Stäbchen, Staphylococcus aureus |
| Liquor-Rhinorrhoe (Liquor-Leck) | Streptococcus pneumoniae, Gramnegative Stäbchen, Haemophilus influenzae |
| Lymphom | Listerien |
| Offene Schädelfraktur oder Kraniotomie | Gramnegative Stäbchen, Staphylokokken, Streptococcus pneumoniae, Haemophilus influenzae |
| Otitis, paranasale Sinusitis | Streptococcus pneumoniae, Haemophilus influenzae, Anaerobier |
| Pneumonie | Streptococcus pneumoniae, andere Streptokokken, Neisseria meningitidis |
| Sichelzellenanämie | Streptococcus pneumoniae, Salmonellen, Neisseria meningitidis, Haemophilus influenzae |
| Splenektomie | Streptococcus pneumoniae, Neisseria meningitidis, Haemophilus influenzae |
| Rezidivierende Meningitis | Streptococcus pneumoniae, Haemophilus influenzae, Neisseria meningitidis |
Tabelle 9 - Semiempirische Therapie der community akquirierten Meningitis (nach Gramfärbung)
|
Gramfärbung |
antibiotische Therapie |
| grampositive Kokken | Drittgenerations-Cephalosporin, evtl. Penicillin, USA: Vancomycin + Drittgenerations-Cephalosporin |
| gramnegative Kokken | Penicillin G |
| grampositive Stäbchen | Ampicillin |
| gramnegative Stäbchen | Breitspektrum Cephalosporin (+ evtl. Aminoglykosid) oder Carbapenem |
Tabelle 10 - Erregerorientierte antibiotische Therapie
|
Erreger |
Therapie der 1. Wahl |
Alternativtherapie |
| Bacteroides fragilis | Metronidazol | Chloramphenicol |
| Enterobacteriaceae | Cephalosporin der 3. Generation + Aminoglykosid | Carbapenem |
| Enterokokken | Ampicillin + Aminoglykosid | Vancomycin |
| H. influenzae Typ B - Beta-Lactamase negativ | Ampicillin | Cephalosporin der 3. Generation |
| H. influenzae Typ B - Beta-Lactamase positiv | Cephalosporin der 3. Generation | |
| Listeria monocytogenes | Ampicillin | Penicillin G |
| Neisseria meningitidis | Penicillin | Ampicillin oder Cephalosporin der 3. Generation |
| Pseudomonas aeruginosa | Ceftazidim + Aminoglykosid | Piperacillin + Aminoglykosid oder Ciprofloxaxin (oder Carbapenem) |
| Staphylococcus aureus, epidermidis | Oxacillin, + evtl. Rifampicin oder Fosfomycin | Fosfomycin + Rifampicin (oder Vancomycin + Rifampicin) |
| Koagulase neg. Staphylokokken | Vancomycin | |
| Streptococcus pneumoniae, Penicillin empfindlich | Penicillin G | Cephalosporin der 3. Generation |
| Streptococcus pneumoniae, teilresistent gegenüber Penicillin | Cephalosporin der 3. Generation | Chloramphenicol |
| Streptococcus pneumoniae, Penicillin resistent | Vancomycin + Cephalosporin der 3. Generation | Chloramphenicol |
| Gruppe B Streptokokken | Penicillin G | Ampicillin oder Cephalosporin der 3. Generation |
Tabelle 11 - Dosierung der antibiotischen Therapie
|
|
Erwachsene (Tagesdosis und
Dosierungsintervall) |
Kinder (Tagesdosis in mg/kg KG und
Dosierungsintervall) |
| Ampicillin | 6-20 g (4 Std.) | 300-400 (4 Std.) |
| Azlozillin | 15-20 g (6-8 Std.) | 200 (6 Std.) |
| Cefotaxim | 6-12 g (8 Std.) | 200 (8 Std.) |
| Ceftazidim | 6-12 g (8 Std.) | 200 (8 Std.) |
| Ceftriaxon | 2-4 g (24 Std.) | 80-100 (24 Std.) |
| Chloramphenicol | 3-4 g (6 Std.) | 100 (6 Std.) |
| Ciprofloxacin | 800-1200 mg (8-12 Std.) | |
| Cotrimoxazol | 960 mg (12 Std.) | |
| Flucloxacillin | 10-20 g (4 Std.) | |
| Fosfomycin | 12-24 g (8 Std.) | 200-300 (8 Std.) |
| Gentamycin, Tobramycin | 240-360 mg (8 Std.) | 5 (8 Std.) |
| Meropenem | 6 g | |
| Metronidazol | 2000 mg | 15, über 1 Std., dann 30 (6 Std.) |
| Mezlozillin | 15-20 g | |
| Penicillin G | 20-40 Mio E (4 Std.) | 250000 E (4 Std.) |
| Piperacillin | 12-20 g (8 Std.) | 200-300 (8 Std.) |
| Rifampicin | 600 mg (1 mal) (10mg/kg KG) | |
| Teicoplanin | 400 mg (8 Std.) | |
| TMP-SMZ (Trimethroprim-Sulfamethoxazol) | 480 mg + 2400 mg (8 Std.) | 10/50 (8 Std.) |
| Vancomycin | 2-3 g (6 Std.) | 40 (6 Std.) |
Behandlungsdauer der antibiotischen Therapie
* Meningokokken werden 7-10 Tage,
* Pneumokokken 10-14
Tage,
* HiB 7-14 Tage,
* Listerien 3-6 Wochen,
* Gruppe B
Streptokokken,
* Staphylokokken,
* gramnegative Stäbchen bis zu 3
Wochen
Eine Lumbalpunktion 24-48 Stunden nach Antibiotikabeginn ist zu empfehlen, vor allem um die Sterilisierung des Liquors feststellen zu können. Zu diesem Zeitpunkt ist die Zellzahl im Liquor nicht selten noch weiter angestiegen und die Gramfärbung kann noch positiv sein, wenngleich die Kultur negativ bleibt, da die in der Gramfärbung gesehenen Erreger nicht mehr vermehrungsfähig sind. Die nach Beendigung der Antibiotikatherapie durchgeführte abschließende Lumbalpunktion unterstützt den klinischen Eindruck, die Afebrilität und die Normalisierung der Entzündungsparameter im Serum (Leukozytenzahl, CRP). Ein persistierendes Fieber über 10 Tage ist praktisch nie durch die Meningitis selbst bedingt, sondern muss Anlass geben, nach anderen Ursachen zu suchen, wie z.B. subdurales Empyem, extrazerebrale infektiöse Foci, medikamenteninduziertes Fieber, etc. (Tabelle 12).
Ein guter Therapieerfolg ist gegeben, wenn der Liquor innerhalb von 24 Stunden steril wird, die Liquor-glukose nach 3 Tagen 40 mg/dl erreicht und das Liquoreiweiß nach 5-7 Tagen wieder im Normbereich ist, Fieberfreiheit besteht und die Zellzahl im Liquor unter 30/mm3 liegt. Zur Entlassung aus dem Krankenhaus muss eine komplette Normalisierung der Laborwerte nicht abgewartet werden - entscheidend ist, neben o.a. Laborparametern, der klinische Verlauf und Zustand.
Tabelle 12 - Ursache für ein prolongiertes Fieber bei einer akuten bakteriellen Meningitis
| Resistenter Erreger | |
| Fehler in der antibiotischen Therapie (Unterdosierung, zu kurze Dauer) | |
| Keimwechsel | |
| intrakranielle Komplikationen | subduraler Erguss sub-, epidurales Empyem Zerebritis, Hirnabszess Schädelosteomyelitis, Mastoiditis Hydro (Pyo)-cephalus mit gestörter Liquordynamik septische Sinunsvenenthrombose zirkumskripte Meningitis |
| septische Absiedelung in andere Organe | Pleuraempyem Endokarditis septische Arthritis Perikarditis |
| Medikamentenunverträglichkeit (sog. drug induced fever) | |
| Rezidiv nach Beendigung der Antibiotikatherapie | |
Adjuvante Therapie
Bakteriologisch wirkende Antibiotika setzen bakterielle Zellwandbestandteile in überwältigender Menge frei, diese führen zu einer akuten Stimulation der inflammatorischen Kaskade mit Freisetzung von Zytokinen (TNF alpha, Interleukin 1, u.a.) und Prostaglandinen. Aus diesem Grund könnte es möglich sein, dass eine Reduktion der Entzündungsantwort im Subarachnoidalraum mittels inflammatorischer Agenzien, gemeinsam mit der Antibiotikatherapie, den Verlauf und das Langzeitergebnis bei einem Patienten mit einer community akquirierten bakteriellen Meningitis günstig beeinflusst. Unter dieser Vorstellung wurde in bisher 9 randomisierten doppelblinden Studien Dexamethason verabreicht. Bei Säuglingen und Kindern ist Dexamethason imstande, die postmeningitische Hörminderung/Taubheit (sensorineurale) signifikant zu reduzieren. Eine tägliche Dosis von 10-12 mg/m2 Körperoberfläche (= 0,6 mg/kg Körpergewicht), auf 4 Tagesdosen aufgeteilt, wird für die Dauer von 3-4 Tagen empfohlen. Wenn Kortikosteroide verabreicht werden, sollen sie unmittelbar vor oder zumindest gleichzeitig mit der ersten intravenösen Dosis des Antibiotikums verabreicht werden. Eine Studie zeigte, dass erwachsene Patienten, die Dexamethason erhielten, eine geringgradig niedrigere Mortalitätsrate bei Pneumokokken-meningitis aufwiesen. Weitere Studien sind derzeit im Laufen, die Ergebnisse müssen abgewartet werden, bevor eine definitive Empfehlung zum Gebrauch von Dexamethason bei erwachsenen Patienten mit einer community akquirierten Meningitis gegeben werden kann.
Neben den Kortikosteroiden wurden nichtsteroidale antiinflammatorische Substanzen, Prostaglandin-inhibitoren, Antiendotoxin-bindende Substanzen, monoklonale Antikörper gegen Endotoxin, Adhäsionsmoleküle, Zytokine, etc., Tumor-Nekrose-Faktor alpha-Antagonist (Pentoxifyllin), Thalidomid, welches imstande ist die TNF-alpha-Freisetzung zu blockieren, sowie Antioxidantien verabreicht, ohne jedoch das Ergebnis zu beeinflussen. Die maximal mögliche Flüssigkeitsrestriktion bei Kindern führt eher zu einer Verschlechterung des Verlaufs und der Langzeitergebnisse einer kindlichen bakteriellen Meningitis. Letztlich ist darauf hinzuweisen, dass bei bakterieller Meningitis durch multiresistente Pneumokokken durch eine Reduktion der meningealen Inflammation und damit Reduktion der Durchlässigkeit der Bluthirnschranke (z.B. durch Steroide) es nicht möglich ist, ausreichende Liquor-Vancomycinspiegel zu erreichen.
Interdisziplinäre Therapie
Ein Patient mit einer bakteriellen Meningitis und einem begleitenden Sepsissyndrom bedarf aggressiver und invasiver intensiv-medizinischer Maßnahmen, wie z.B. zentral-venöser Katheter, eventuell sogar Pulmonalis-Katheter (Swan-Ganz-Katheter), frühzeitige Intubation und kontrollierte Beatmung, ausreichendes und kontrolliertes Flüssigkeits- und Elektrolytmanagement, ausreichende Analgo-sedierung und frühzeitige parenterale, so rasch wie möglich jedoch auf enteral umgestellte Ernährung.
Therapie der Komplikationen
Erhöhter Hirndruck
Wenngleich nur ca. 5% der
Patienten mit einer akuten bakteriellen Meningitis massiv erhöhte
Hirndruckwerte (bis zu 50 Hg) aufweisen, besteht eine leichte bis
mäßiggradige Hirndruckerhöhung beim Großteil dieser Patienten.
Rechtzeitiges Erkennen und ebenso rechtzeitige Therapie sind
essentiell.
Er erhöhter Hirndruck kündigt sich mit Bewußtseinsstörung, vegetativen Symptomen (Erbrechen) an, bei Fortschreiten wird der Patient komatös, eine Mydriasis mit fehlender Lichtreaktion der Pupillen, Dekortikations- und Dezerebrationsschablonen, sowie Sistieren der Hirnstammreflexe sind die entsprechenden klinisch neurologischen Korrelate des weiteren Fortschreitens des intrakraniellen Druckes. Da die Hirndruckentwicklung sehr rasch vor sich geht, ist eine Stauungspapille (Papillenödem) nur sehr selten (< 1%) zu sehen. Bei erhöhtem intrakraniellen Druck führt eine Lumbalpunktion zur Beschleunigung der transtentoriellen und letztlich transforaminellen Herniation. Neben dem für eine bakterielle Meningitis typischen diffusen Hirnödem, kann ein Hydrocephalus (Pyocephalus) für eine Hirndruckerhöhung hauptverantwortlich sein. Dieser erfordert schnellstmöglich eine externe Ventrikel-drainage zur Hirndruckreduzierung. Die Therapie des zur Hirndruckerhöhung führenden Hirnödems ist in Tabelle 13 angeführt.
Tabelle 13 - Behandlung des erhöhten Hirndrucks
| 1. Hydro-, Pyocephalus: externe Ventrikeldrainage |
| 2. Oberkörperhochlagerung (30°) |
| 3. Hyperventilation, PaCO2 zwischen 30 und 35 mmHg |
| 4. Osmotherapie: z.B. Mannit (250-500 mg/kg KG jeweils bei Bedarf als Bolus) |
| 5. Barbiturattherapie (evtl. Propofol): initiale Dosis 1 mg/kg KG/min, Gesamtdosis bis zu 500 mg. Erhaltungsdosis 1-3 mg/kg KG/Std. Titrierung der Erhaltungsdosis nach EEG |
| 6. Steroide (Dexamethason)? |
Bei einer akuten bakteriellen Meningitis ist ein diffuses Hirnödem meist eine Kombination eines vasogenen, zytotoxischen und interstitiellen Ödems. Ein zusätzliches Sepsissyndrom aggraviert die vasogene, ein Hydrocephalus die interstitielle Komponente. Sowohl ein Sepsissyndrom, als auch ein frühzeitiges intensivmedizinisches Management, insbesondere rasche Intubation und mechanische Ventilation. Obwohl eine aggressive Hyperventilation (PaCO2 < 25 mmHg) zu einer vorübergehenden weiteren Hirndrucksenkung beitragen kann, ist großer Wert darauf zu legen, dass PaCO2-Werte < 30 mmHg nicht erreicht werden, da im Rahmen der Entzündungskaskade die zusätzliche, durch die Hyperventilation erreichte Vasokonstriktion, den Vasospasmus aggravieren und zur fokalen oder diffusen Hirnparenchym-Ischämie führen könnte. Eine Osmotherapie mit Mannit (oder Glyzerol oder Sorbit) darf nur als Bolustherapie unter Aufrechterhaltung einer Serumosmolarität um 320 mOsm/L durchgeführt werden. Eine mehr als 48 Stunden lange Mannittherapie führt durch Einwanderung der osmotisch wirksamen Mannitmoleküle in den intrazellulären Raum zum Reboundphänomen und möglicherweise zur Verschlechterung des Hirnödems in der Spätphase. Eine Barbiturattherapie (Pentobarbital, Thiopental) wird nur unter engmaschigster EEG-Kontrolle - bis zum Erreichen eines "burst supression Musters" - durchgeführt. Größter Wert ist auf die Hautpflege zur Vermeidung von "Barbituratblasen" zu legen. Wenngliche Steroide (Dexamethason) imstande sind, zumindest unter den experimentellen Bedingungen des Tierversuches, das vasogene und interstitielle Ödem günstig zu beeinflussen, ist der Einsatz von Dexamethason zur Hirnödemtherapie bei schwerster bakterieller Meningitis derzeit (noch) nicht gerechtfertigt. Die Permeabilität zerebraler Kapillarendothelien (Bluthirnschranke) wird durch Dexamethason gesenkt und damit das vasogene Hirnödem reduziert. Möglicherweise führt dieser Mechanismus jedoch zu einer Verschlechterung der Penetration der Antibiotika durch die Bluthirnschranke. Da bei deutlich gesteigertem intrakraniellen Druck der Perfusionsdruck nur schwer aufrecht erhalten werden kann, vor allem bei Patienten, die im Rahmen eines begleitenden Sepsis-syndroms eine arterielle Hypotonieneigung zeigen und auch auf hohe Dosen von Katecholaminen nicht mehr ausreichend ansprechen, kommt es zur Minderperfusion des Gehirns und damit zu einer doppelt bedingten Reduktion des Antibiotika-Angebotes im intrakraniellen Raum.
Eine bilaterale Kraniotomie mit Duraerweiterungsplastik, ist im Einzelfall als ultima ratio zu diskutieren.
Hydrocephalus
Ein Hydrocephalus aresorptivus
bzw. ein Hydrocephalus occlusus (Pyocephalus) führt zu rasch steigendem,
lebensbedrohlichem intrakraniellen Druck. Eine raschestmögliche externe
Ventrikel-drainage, die bei Pyocephalus eventuell bilateral angelegt
werden muss (bei Okklusion des 3. Ventrikels), führt zur prompten
Hirndrucksenkung.
Zerebrale Krampfanfälle
Bei bis zu 30% der
Patienten (besonders Kinder und Erwachsene mit Pneumokokkenmeningitis)
kommt es in den ersten Tagen ihrer Erkrankung zu meist generalisierten
tonisch klonischen Anfällen. Schwere bzw. langdauernde Anfälle,
insbesondere ein generalisierter tonisch klonischer status epilepticus
sind per se lebensbedrohliche Krankheitsbilder und verschlechtern die
Prognose. Eine raschest mögliche Applikation von Diazepam 10-20 mg i.v.
bei Bereithaltung des Intubationsinstrumen-tariums unterbricht den tonisch
klonischen Anfall. Sollten die tonisch klonischen Aktivitäten nach 20 mg
Diazepam (oder Lorazepam) nicht sistieren, wird Diphenylhydantoin in der
Dosis von 250 mg i.v. gegeben. Diese Dosis kann bis zur Gesamtdosis von
1000 mg wiederholt werden. Wenn das Anfalls-geschehen auch mit dieser
sequentiellen Therapie nicht unterbrochen werden kann, bedarf es einer
Barbituratnarkose. Spätestens zu diesem Zeitpunkt ist der Patient
intubationspflichtig.
Flüssigkeits- und Elektrolytmanagement
Eine
Flüssigkeitsrestriktion ist unter keinen Umständen indiziert, sie führt
zur Verschlechterung der Prognose. Andererseits führt ein SIADH (bei
Kindern nicht selten beobachtet) zur Hyponatriämie, deren Ausmaß und Dauer
mit dem Auftreten neurologischer Langzeitschäden korreliert. Aus diesem
Grunde ist es eine, nur auf Intensivstationen durchzuführende ausgewogene
Bilanzierung des Flüssigkeits- und Elektrolythaushaltes essentiell.
Engmaschigste Elektrolytkonzentrationsmessungen im Serum und im Harn sind
unabdingbar notwendig. Bei Hyponatriämien von < 130 mEq/l ist die
Natriumzufuhr vorsichtig, aber kontinuierlich notwendig, 1-2 stündliche
Elektrolytkontrollen verhindern zu rasches Anheben des
Serum-Natriumspiegels und damit die Gefahr einer pontinen Myelinolyse.
Subdurale Ergüsse
In seltenen Fällen kompliziert
ein raumfordernd wirksamer subduraler Erguss eine bakterielle Meningitis.
Dieser, oder wenn Hinweise für ein subdurales Empyem (siehe dort)
bestehen, erfordert nur bei raumfordernder Wirkung eine neurochirurgische
Intervention (externe Ableitung).
Therapie der Vaskulitis (Arteritis)
Neben dem
diffusen Hirnödem führt eine Lumenseinengung im Rahmen vaskulitischer
Prozesse zu einer zusätzlichen Reduktion der zerebralen Perfusion und
damit zur Ischämiegefahr. Bevor das Fortschreiten des intrakraniellen
Druckes zu einem Zusammenbrechen der zerebralen Autoregulation führt, kann
eine Vaskulitis (Vasospasmus) - bedingte Lumenseinengung der Gefäße
eventuell mit einer Triple H-Therapie (Hypertonie, Hypervolämie,
Hämodilution) - in Anlehnung an die Vasospasmustherapie der
Subarachnoidalblutung - behandelt werden. Kardiopulmonales Monitoring
(evtl. mit Swan-Ganz-Katheter) ist bei der Triple H-Therapie unerlässlich.
Katecholamine (Dopamin, Dobutrex, Arterenol, Neosynephrine),
Flüssigkeitsmengen (Ringerlaktat, NaCl, etc.) bis zu 10 (15) Liter pro
Tag, sowie Hämodilution mit Hydroxyäthylstärke stellen das
intensivmedizinische Grundgerüst der Triple H-Therapie dar. Neben dem
kardiopulmonalen Monitoring ist ein engstes Monitoring der
Flüssigkeits-bilanz und der Elektrolyte unbedingt notwendig.
Septische Hirn-/Sinusvenenthrombose
Obwohl keine
etablierten Studien über die Wirksamkeit der bei blander Sinusthrombose
akzeptierten Vollheparinisierung bestehen, wird diese empfohlen, da bei
alleiniger antibiotischer Therapie die Mortalität einer septischen
Sinusvenenthrombose bei über 50% liegt.
Prognose
Die Prognose der bakteriellen Meningitis wird durch das Alter des Patienten, den Erreger, die neurologische Symptomatik (Bewusstseinsstörung), die systemische Hypotonie (Sepsissyndrom) zum Zeitpunkt des Beginns der antibiotischen Therapie, vom Zeitraum des Beginns der Erstsymptome bis zur Diagnosestellung, von der adäquaten antibiotischen Therapie und vor allem von einer ausreichenden supportiven Therapie bestimmt.
Während in der Vorantibiotika-Ära Mortalitäten von 70-100% bei bakterieller Meningitis beschrieben werden, hängen die Mortalitätsraten in der Antibiotika-Ära neben den oben angeführten Prognose- verschlechternden Faktoren, vor allem vom Erreger und vom Alter des Patienten ab: bei Säuglingen bestehen (erregerunabhängig) Sterblichkeitsraten von 10-25%, bei Kleinkindern und Kindern von 3-7% und bei Erwachsenen von 10-25%. Erregerunabhängig finden sich Mortalitätsraten bei Pneumokokken-meningitis von 19%, bei Meningokokkenmeningitis von 13% (bei Meningokokkenmeningitis 5-10%, bei begleitender oder vorwiegender Meningokokkensepsis bis zu 25%) und bei HiB-Meningitis von 3%. Diese Letalitätszahlen sind Durchschnittswerte, regional Letalitätsraten differieren zum Teil beträchtlich (Meningokokken: 4-10%, Pneumokokken 12-24%, HiB 2-5%). Die Mortalität steigt insbesondere bei älteren Patienten, bei initial komatösen Patienten (Verdreifachung der Mortalität) und bei initialen tonisch klonischen Anfällen. 98% der Patienten, die an der bakteriellen Meningitis versterben, weisen zumindest einen dieser drei Faktoren (Alter > 60 Jahre, initiale Bewusstseinsstörung, zerebrale Krampf-anfälle) auf. Eine community akquirierte Meningitis trägt eine niedrigere Mortalität als eine nosokomiale Meningitis.
Meningokokken
Chemoprophylaxe
Die Meningokokkenübertragung erfolgt meist bei engem Kontakt, Kinder unter 3 Jahren sind jedoch kaum Keimträger. Das Risiko einer Übertragung von Meningokokken im engen familiären/häuslichen Bereich ist 500- bis 800-fach erhöht, wobei der räumliche Abstand zur erkrankten Person direkt mit dem Infektionsrisiko korreliert. Grundsätzlich gilt, wie bei HiB, dass nur Patienten mit einem "kissing mouth"-Kontakt eine Chemoprophylaxe verabreicht bekommen sollen. Ein "kissing mouth"-Kontakt bedeutet, dass eine Person mit dem Indexfall mindestens vier Stunden pro Tag kontinuierlich im selben Raum verbracht hat. In Schulen, Kindergärten, Heimen und Kasernen ist eine Prophylaxe nur bei einer Häufung von Meningokokkenerkrankungen bzw. Epidemien indiziert. Rifampicin, 2 x 600 mg durch 2 Tage hindurch, hat eine Keimträgereradikationsrate von mehr als 90%. Eine Kombination mit Doxizyklin (2 x 100 mg bei Erwachsenen) erreicht eine Eradikationsrate von über 99%. Als Alternativen kommen Ciprofloxaxin (2 x 400 mg täglich durch 4 Tage) oral oder Ceftriaxon (bei Schwangerschaft) in Frage. Da durch die konventionelle Meningitistherapie (z.B. Penicillin G intravenös) die Meningokokken nicht zuverlässig aus dem nasopharyngealen Raum eliminiert werden, wird vor der Entlassung aus dem Krankenhaus eine Rifampicinprophylaxe beim Patienten selbst empfohlen (Dosis siehe oben). Kranken-hauspersonal und notfallmedizinische Erstversorger sollen nur bei engstem Kontakt mit dem Patienten (z.B. Mund-zu-Mund-Beatmung, Intubation) einer Chemoprophylaxe zugeführt werden.
Immunprophylaxe
Ein tetravalenter Impfstoff gegen die Gruppen A, C, Y und W 135 steht zur Verfügung. Nur exponierte Personen sollen geimpft werden, z.B. Reisende in Epidemiegebiete oder Hochendemiegebiete Afrikas, Südasiens und eventuell Südamerikas, sowie engste Kontaktpersonen eines an einem dieser Serotypen Erkrankten.
Pneumokokken
Chemoprophylaxe
Eine Chemoprophylaxe ist nur bei Kindern mit Mucoviszidose, bei Splenektomierten, bei Patienten mit nephrotischem Syndrom, Sichelzellenanämie und anderen immunsuppressiven Erkrankungen bzw. Zuständen indiziert. Für Patienten mit Liquorfistel zeigt eine Chemoprophylaxe keine Wirksamkeit. Es wird Penicillin oral mit einer Dosis von 60.000 Einheiten/kg KG/Tag (aufgeteilt auf 3 Einzeldosen) für die Dauer von 1 Woche verabreicht. Im Nasopharyngealraum kommt es nur bei ca. 60% zu einer Kolonisie-rungssverhinderung.
Immunprophylaxe
Der 23-valente Impfstoff deckt die wesentlichen Serotypen (der insgesamt 84) ab, alle eine Meningitis verursachenden Serotypen sind inkludiert. Bei unter 2-Jährigen ist der Antikörperanstieg unzuverlässig. Der Impferfolg bei Erwachsenen beträgt 90-95%, der Impfschutz beträgt 5-8 Jahre. Die Immunisierung wird bei älteren Menschen, immunsupprimierten Menschen, z.B. Diabetes mellitus, vor allem aber bei Patienten mit angeborener Asplenie oder Zustand nach Splenektomie bzw. bei funktioneller Hypo- oder Asplenie (z.B. bei Sichelzellenanämie oder Thalassämie) empfohlen. Der Impferfolg wurde bisher an der Reduktion von pulmonalen Pneumokokkeninfekten gemessen, eine Reduktion der Pneumokokken-meningitis war nie Gegenstand einer wissenschaftlichen Untersuchung. Eine operative Sanierung von Liquorfisteln, Knochen- oder Duralücken ist essentiell.
Literatur
E. Schmutzhard (2000): Entzündliche Erkrankungen des Nervensystems. Thieme Verlag, Stuttgart